-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Dokážeme včasně diagnostikovat poruchy polykání?
Časný screening poruch polykání, kazuistiky
Are we able to diagnose swallowing disorders in time?
We present several case studies that illustrate the diversity of aetiology of swallowing disorders and point out the need for early detection of problems. We also present the most commonly used tests for screening and differential diagnosis of dysphagia. In all these cases dysphagia had significant impact on the nutritional status of patients and in most cases led to significant health complications.
Key words:
swallowing disorders – swallowing tests – eating assessment tool EAT-10
Autoři: MUDr. Pavlína Malochová; MUDr. Pavla Mádlová; MUDr. Tomáš Richter; Prof. MUDr. Eva Topinková, CSc.
Působiště autorů: Geriatrická klinika 1. LF UK a VFN, Praha
Vyšlo v časopise: Geriatrie a Gerontologie 2013, 2, č. 3: 165-170
Kategorie: Kazuistiky
Souhrn
Prezentujeme několik kazuistik, které dokreslují etiologickou rozmanitost poruch polykání a poukazují na nutnost časné detekce obtíží. Uvádíme také nejčastěji používané testy pro screening a diferenciální diagnostiku dysfagie. U všech uvedených případů měla dysfagie významný vliv na nutriční stav pacientů, u většiny vedla k významným zdravotním komplikacím.
Klíčová slova:
poruchy polykání – testy polykání – subjektivní test EAT-10Kazuistika 1
Anamnéza. 61letý pacient byl hospitalizován na Geriatrické klinice pro malnutrici při stavu po neradikální resekci pro karcinom jazyka s následnou radioterapií. Operace byla provedena v roce 2004, od roku 2010 byl zaveden PEG, zjištěna tracheoezofageální píštěl, opakované aspirace, potravu přijímá jen via PEG. Postupně zhoršování řeči, po každém polknutí se objevuje kašel.
Výsledky vyšetření. ADL: 100 bodů, MMSE: 29 bodů, úbytek hmotnosti za poslední 3 měsíce 7 kg, hmotnost 68 kg, BMI: 17. Mini Nutritional Assessment (MNA): 11 bodů – podvýživa. Biochemie – parametry nutrice: albumin 37,1 g/l, celková bílkovina 62,7 g/l.
Testy polykání. EAT-10 : 38 bodů – porucha polykání, test Mandysové: 3 body – přítomnost dysfagie, test Danielsové: 4 body – pravděpodobná aspirace, GUSS: 0 bodů – vysoké riziko aspirace.
Provedeno ORL vyšetření s videoendoskopií (flexible endoscopic evaluation of swallowing – FEES) s nálezem: nosohltan bez patologie, choany volné, kořen jazyka atrofický, valleculy se stagnací hlenů, s bělavými povlaky, epiglottis v celé šířce prosáklá, ztluštělá, fixovaná, při polknutí se nepřeklápí, pouze s minimálním pohybem. Nitro hrtanu volné, hlasivky hybné, nedomykavost ve střední 1/3, menší exkurse vlevo, subglottis volná. Při polknutí vody patrná fixace epiglottis a přetékání tekutiny do hrtanu bez následného kašle. Výrazná dysfagie při polykání tekutin, tuhá sousta nezkoušena. Fixace glottis. Doporučena dále jen neorální výživa a hydratace.
Další průběh. Během hospitalizace byla antibiotiky léčena aspirační pneumonie s dobrým klinickým efektem, hydratace přechodně doplňována i parenterálně. Při zhoršení celkového stavu regurgitoval žaludeční obsah do dýchacích cest, proto sníženy jednotlivé dávky Nutrisonu, dodržována elevace horní poloviny těla s výrazným zlepšením tolerance aplikací do PEG. Pacient byl po přeléčení propuštěn domů, je sledován v ambulanci nutriční péče.
Závěr. Kazuistika dokumentuje správnou výpovědní hodnotu použitých screeningových testů polykání, jejich výsledky odpovídaly těžké poruše polykání s aspirací. Aspirace byla potvzena provedením instrumentálního vyšetření.
Kazuistika 2
Anamnéza. 88letý pacient byl přijat na Geriatrickou kliniku pro stav po urosepsi a stavy zmatenosti. Do hospitalizace žil se svou výrazně mladší a vysokoškolsky vzdělanou manželkou, která vedla domácnost, společně podnikali i dlouhé zahraniční výlety. Při procházkách se v posledních měsících začaly objevovat chvilkové zárazy v chůzi a krátké stavy dezorientace. Mentální stav manželka hodnotila jako velmi dobrý, předčítali si knihy, o kterých si společně povídali, popírala přítomnost kognitivního deficitu před hospitalizací. Pacient byl léčen pro diabetes mellitus 2. typu perorálními antidiabetiky, pro sick sinus syndrom měl od roku 2009 implantován kardiostimulátor, nyní byla základním rytmem chronická fibrilace síní s klidným převodem na komory.
Při přijetí byl bradypsychický, komunikoval jen krátce, časově dezorientovaný, imobilní. Byla přítomna výrazná porucha polykání. Při doplňování anamnézy manželka nejprve popírala obtíže s polykáním, postupně však sama sdělila, že „ manžel již několik měsíců nechce řádně jíst, a tak mu často váznoucí sousto sama posouvá dále do krku, nyní trochu zhubl, býval více při těle“. Obtížím nepřikládala větší význam, u lékaře to neřešili. Měla pocit, že jí to manžel dělá naschvál.
Výsledky vyšetření. ADL: 5 bodů, MMSE: 11 bodů, Mini Nutritional Assessement (MNA): 8 bodů – podvýživa. Biochemie – parametry nutrice: albumin 35,4 g/l, celková bílkovina 58,5 g/l.
Testy polykání. EAT-10 : 28 bodů – porucha polykání, test Mandysové: 4 body – přítomnost dysfagie, test Danielsové: 4 body – pravděpodobná aspirace, GUSS: 2 body v přímém testu – vysoké riziko aspirace.
Bylo provedeno neurologické vyšetření s nálezem centrální léze n. hypoglossus vlevo, centrální parézou n. facialis, oslabením levostranných končetin. Nalezeny pozitivní axiální jevy, pacient bez fatické poruchy, bez dysartrie. CT mozku prokázalo pokročilou celkovou atrofii bez čerstvých ložiskových změn denzity. Neurologickým konziliem bylo pro pseudobulbární syndrom doporučeno zavedení PEG. Pacientovi byla dále zavedena nazogastrická sonda, kterou však pacient ještě týž den extrahoval. Hydratace zajišťována parenterálně. K plánovanému zavedení PEG nedošlo pro rozvoj aspirační pneumonie s následným úmrtím.
Závěr. Zajímavostí této kazuistiky je dlouhé přehlížení polykacích obtíží bez vyhledání odborné péče. Vyplývá z ní skutečnost, že povědomí laické veřejnosti o polykacích obtížích je nízké, poukazuje na značný prostor pro širší informování o příznacích, diagnostice a možnostech terapie poruch polykání. Přínosným může být širší využívání samohodnoticího dotazníku EAT-10 v ambulancích i čekárnách lékařů první linie.
Kazuistika 3
Anamnéza: 84letý pacient s Alzheimerovou chorobou s postupně progredující poruchou paměti, řeči, ztrátou orientace a stavy agitovanosti byl z domova přijat pro poruchu příjmu potravy. V anamnéze v roce 1998 diagnostikována achalázie jícnu, v letech 2006–7 opakovaně dilatace, poslední 2 roky zcela bez obtíží, přijímal normální stravu.
Výsledky vyšetření. ADL: 30 bodů, MMSE: 2 body, úbytek hmotnosti za poslední 3 měsíce 5 kg, hmotnost 62 kg, BMI: 19. Mini Nutritional Assessment (MNA) : 12 bodů – podvýživa. Biochemie – parametry nutrice: albumin 37,6 g/l, celková bílkovina 59,5 g/l,
Testy polykání. EAT-10: vzhledem k těžké demenci nelze použít, test Mandysové: žádný abnormální nález, nesvědčil pro dysfagii, test Danielsové: bez abnormálního nálezu svědčícího pro riziko aspirace.
V den přijetí provedeno endoskopické vyšetření, jícen byl vyplněn tekutým i tuhým obsahem, lumen výrazně dilatováno, v distálním úseku 35 cm od řezáků nebylo možné dále pokračovat pro přítomnost tuhé stravy, patrná lividní tkáň. Následně proveden rtg hrudníku a břicha k vyloučení perforace v distálním jícnu. Pro nejednoznačný nález provedeno CT, které perforaci vyloučilo. Doporučeno nepřijímat nic p. o.,podávány inhibitory protonové pumpy v dávce 80 mg i. v/den a parenterální výživa typu all-in-one.
Kontrolní endoskopie provedena za 2 dny. Jícen byl výrazně dilatován, vinutý, v jeho lumen již jen trocha tekutiny. Sliznice v distálním úseku místy pokryty fibrinovými nálety, ve vzdálenosti 40 cm od řezáků bylo lumen kompletně uzavřeno, sliznice živě červená. S mírným tlakem na endoskop se zdařilo proniknout přes oblast stenotické kardie do žaludku, sliznice lehce překrvené, jinak normální nález. Po vodiči provedena dilatace kardie na 30 mm. Výkon proběhl bez komplikací, v den výkonu doporučeny p. o. jen tekutiny, od následujícího dne kašovitá strava. Perorální realimentaci pacient toleroval dobře. Po dalších 4 dnech byla provedena druhá kontrolní gastroskopie, jícen byl nadále dilatovaný, odsáto množství žlutohnědého tekutého obsahu, terminální část jícnu deviována doprava, zprvu nebylo možné vizualizovat lumen. Po dalších pokusech se dařilo celkem volně proniknout stenotickým úsekem kardie do žaludku, který je prostorný, bez zbytků stravy, sliznice intaktní. V inverzi kromě lehce hypertrofických řas v kardii přiměřený nález, v antru normální nález. Pylorus volně prostupný. Po vodiči zaveden dilatační set s balonkem do oblasti kardie a provedena druhá etapa dilatace.
Závěr a doporučení. Pacient postupně převeden na kašovitou stravu. Přeložen do zařízení sociální péče. Dále nutná nejen monitorace příjmu potravy při krmení ošetřujícím personálem, ale také sledování známek eventuální regurgitace stagnujícího obsahu v jícnu. Příznakem může být i nespecifické zhoršení celkového stavu, neklid, zmatenost. Pacient s těžkou kognitivní poruchou není schopen konkretizovat své obtíže, proto je limitováno použití subjektivních dotazníkových nástrojů. Je potřebné sledovat nutriční stav, vhodná je fortifikace stravy nutričními doplňky.
Kazuistika 4
Anamnéza. 94letá pacientka byla přijata z domova po vyšetření na centrálním interním příjmu pro stav po aspiraci stravy – jedla smažený sýr. Pacientka byla po ischemické cévní mozkové příhodě staršího data v povodí ACM l. sin s pravostrannou hemiparézou, dle CT mozku prokázány difuzní ischemické změny obou mozkových hemisfér.
Výsledky vyšetření. ADL: 0 bodů, MMSE: 18 bodů, Mini Nutritional Assessement (MNA): 6 bodů – podvýživa. Biochemie – parametry nutrice: albumin 36 g/l, celková bílkovina 64,7 g/l.
Testy polykání. EAT-10 : 19 bodů – porucha polykání, test Mandysové: 3 body – pravděpodobná přítomnost dysfagie, test Danielsové: 1 bod – nesvědčí pro riziko aspirace, GUSS: 17 bodů – lehká porucha, doporučení kašovité stravy.
Při přijetí byla spavá, krátce probuditelná, s malou spoluprací. Následující den došlo k rozvoji pneumonie vpravo, pro kterou podávána antibiotika s postupným poklesem parametrů zánětu. Krátce po ukončení ATB terapie došlo ke klostridiové infekci s produkcí toxinů a vznikem průjmů. Pacientka byla hydratována parenterálně, po kúře Entizolem průjmy ustaly, celkový stav byl mírně zlepšen. Dobře tolerovala pomalé krmení kašovitou stravou, krmení jen v poloze vsedě v lůžku. K další ošetřovatelské péči byla přeložena na oddělení následné péče.
Závěr. Tato kazuistika dokládá nutnost sledování poruch polykání u pacientů po cévních mozkových příhodách a dále nutnost doporučení vhodné konzistence stravy a edukace nejen pacientů, ale zejména pečujících osob.
Poruchy polykání
Pojem dysfagie označuje poruchu polykání vznikající v průběhu transportu potravy nebo tekutin od úst do žaludku. Jedná se o častý zdravotní problém zejména stárnoucí populace, ve které narůstá výskyt těchto poruch jednak vlivem věkem podmíněných změn ve fyziologii polykání, jednak nárůstem četnosti onemocnění vedoucích k dysfagii.
Prevalence dysfagie u osob nad 65 let se odhaduje v rozmezí 13,5–50 %(1, 2). Zejména vysoká prevalence dysfagie je u onemocnění nervového systému, výskyt při cévních mozkových příhodách je až 50%, u Parkinsonovy choroby 35%, Alzheimerovy choroby 84%, roztroušené sklerózy 44% .
Dysfagie vede k řadě zdravotních komplikací, především k malnutrici(3), zvýšenému riziku dehydratace a výrazně zvýšenému riziku rozvoje aspirační pneumonie. Aspirační pneumonie vznikají až u jedné třetiny pacientů po iktu a jsou vedoucí příčinou úmrtí v postiktovém období. Po akutních cévních mozkových příhodách jsou příčinou přibližně 35 % úmrtí(4).
Příčinou poruch polykání vzhledem ke složitosti polykacího aktu a nutné souhře s respirací může být celá řada onemocnění. Nejčastější jsou neurogenní příčiny – 56,5 %, strukturální primární onemocnění hlavy a krku –15,2 %, následky po chirurgických zákrocích, radioterapii či chemoterapii – 16,1 %. Podle lokalizace poruchy dělíme dysfagie na orofaryngeální a esofageální.
Poruchy polykání mají značný vliv na kvalitu života pacienta, na jeho morbiditu i mortalitu. Vzhledem k závažnosti následků dysfagie a výrazné prevalenci tohoto problému je nutné aktivní vyhledávání počínajících poruch polykání. Vhodné je využití také subjektivních metod hodnocení polykání pacientem, které odrážejí nejen míru potíží při polykání, ale také úroveň kvality života pacienta(5).
Dysfagie může být způsobena funkční nebo strukturální abnormalitou v oblasti ústní dutiny, hltanu, hrtanu, jícnu, případně žaludku, zásadní je také řídicí a koordinační funkce mozku a nervového systému. V rámci diagnostického postupu je po základním klinickém vyšetření potřeba vyšetřit všechny tyto oblasti. Využíváme anamnestické údaje, klinické vyšetření a specializovaná vyšetření. Získáváme informace o příznacích, trvání a charakteru obtíží, sledujeme choroby s vyšším rizikem poruch polykání. Velký význam má údaj nechtěného váhového úbytku, poruchy tvorby hlasu, poruchy fatických funkcí, abnormální kašel, změny hlasu po polykání. Pacienti, kteří přesně definují a lokalizují problém, mají obvykle poruchu v oblasti dutiny ústní a hltanu. Pacienti s esofageální dysfagíí uvádějí neurčité obtíže(2).
Screeningové testy polykání
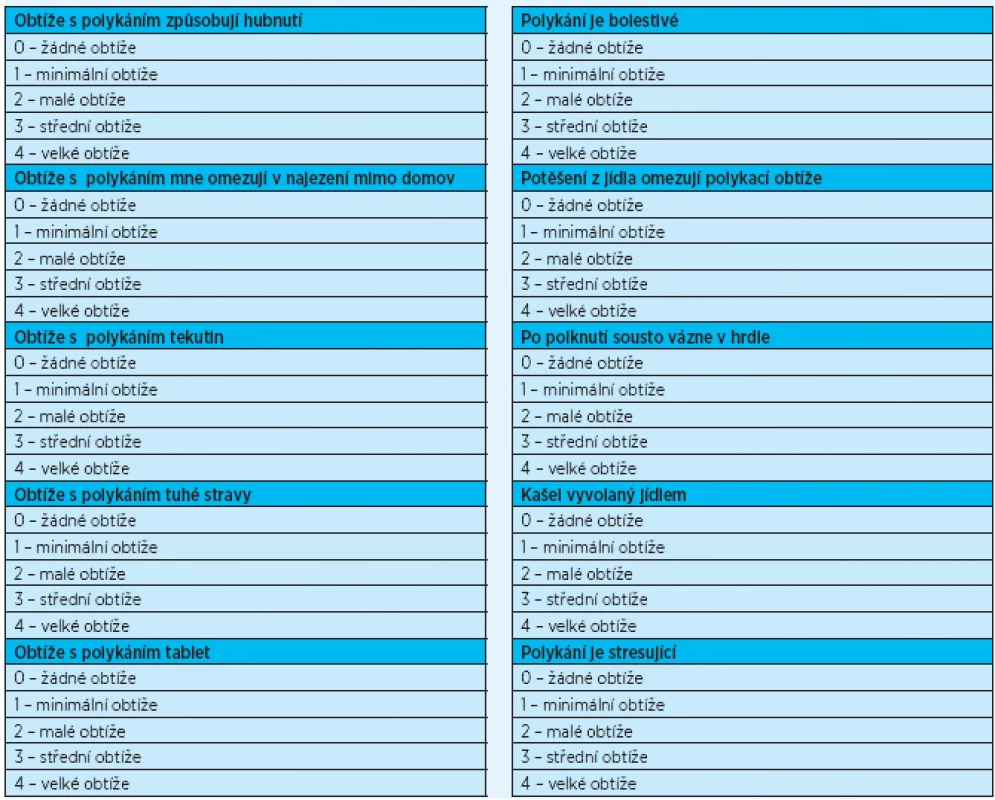
Pro anamnestické vyhledání pacientů s dysfagií je přínosným a jednoduchým nástrojem dotazníkové šetření pomocí EAT-10 (Eating Assesment Tool) (tab. 1), hodnotící subjektivně schopnost polykat(6, 7). Pro svou nenáročnost a možnost vyplnit dotazník i samostatně je tento test velmi vhodný pro testování osob s rizikem poruch polykání v první linii. Jedná se zejména o pacienty s neurologickými onemocněními, křehké geriatrické pacienty, pacienty závislé na ošetřovatelské péči a pacienty s anamnézou opakovaných pneumonií (tab.1). Patologický nález zjištěný tímto dotazníkem je potřeba vnímat jako varovný signál upozorňující na nutnost podrobnějšího vyšetření.
Test se skládá z deseti otázek zjišťujících hubnutí, bolestivost při polykání, omezení společenských aktivit spojených s jídlem, ptá se na obtíže s polykáním tekutin, tuhé stravy, léků, kašel v souvislosti s jídlem a na vliv na psychickou pohodu. Každá položka je hodnocena od nuly do čtyř bodů, od nepřítomnosti obtíží po velké obtíže. Pokud je celkové skóre 3 a vyšší, je pravděpodobná porucha polykání.
Pomocí tohoto dotazníku byl v roce 2012 na Geriatrické klinice VFN Praha testován výskyt poruch polykání na vzorku 70 pacientů, obtíže byly zjištěny u 34,28 % respondentů. Širší využívání tohoto nástroje v praxi by vedlo k dřívějšímu záchytu pacientů s vhodnou intervencí vedoucí ke snížení závažných zdravotních následků.
Klinické testy polykání
Pro záznam vyšetřování polykacích obtíží neexistuje jediný obecně doporučovaný postup. Velká část testů je zaměřena na projevy penetrace a aspirace, nezachycují obtíže v přípravné a orální fázi polykání. Většina testů je určena primárně pro neurologické pacienty, zejména po akutní cévní mozkové příhodě, jedná se o klinické bed-side testy.
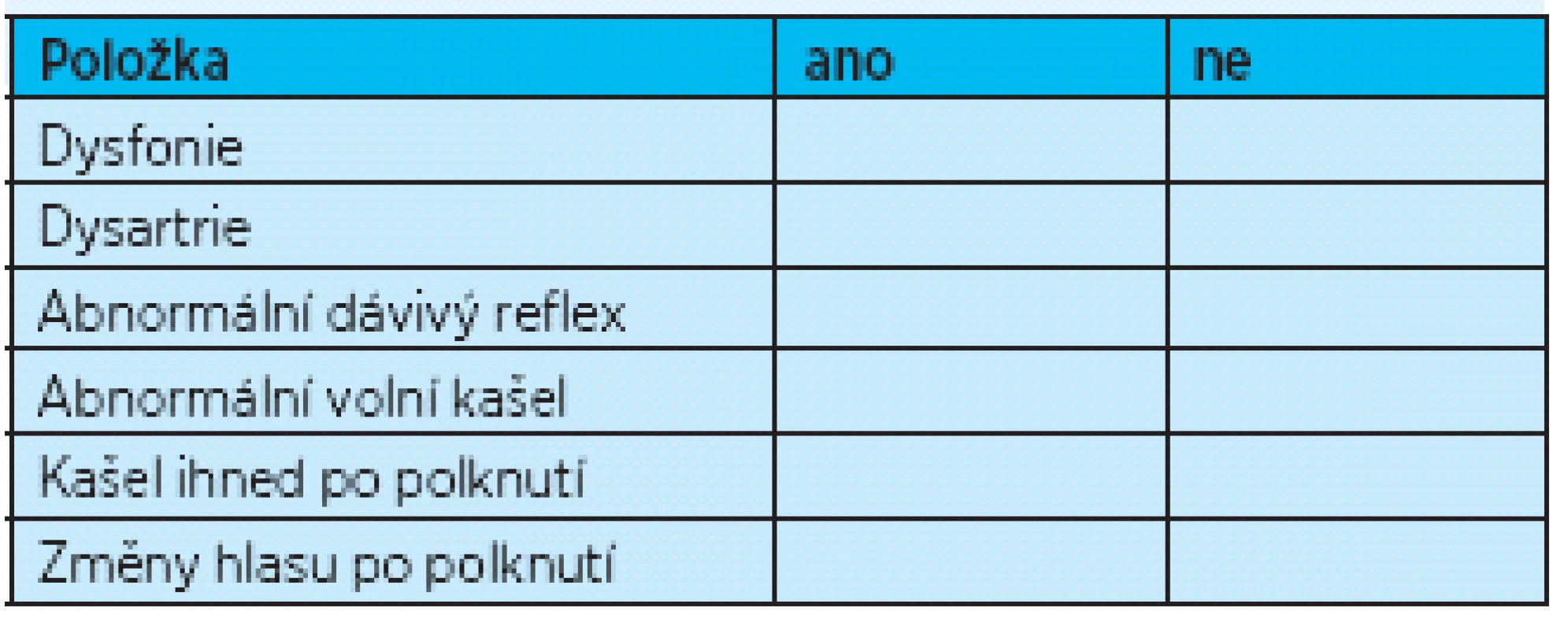
Vyšetření podáním doušku vody je možno zaznamenat pomocí testu Danielsové(8, 9), který sleduje reakci pacienta po podání vody v šesti parametrech (tab. 2). Přítomnost dvou a více parametrů vykazuje 92,3% senzitivitu a 66,7% specificitu pro výskyt aspirace. Test byl vytvořen pro sledování pacientů po akutní cévní mozkové příhodě.
Při orientačním zjišťování přítomnosti poruch polykání je možné použití osmipoložkového nástroje pro testování polykací funkce podle Mandysové (10), který hodnotí schopnost zakašlat, orientačně motorický deficit v oblasti čelistí, jazyka, tváří, ramen, přítomnost dysartrie, afazie a reakci na podání zahuštěné tekutiny (tab. 3). Přítomnost jednoho a více abnormálních výsledků znamená, že pacient má pravděpodobně dysfagii. U neurologických pacientů byla zjištěna senzitivita tohoto nástroje 95,5%, specificita 28,5%.
Tab. 3. Test Mandysové<sup>(10)</sup> 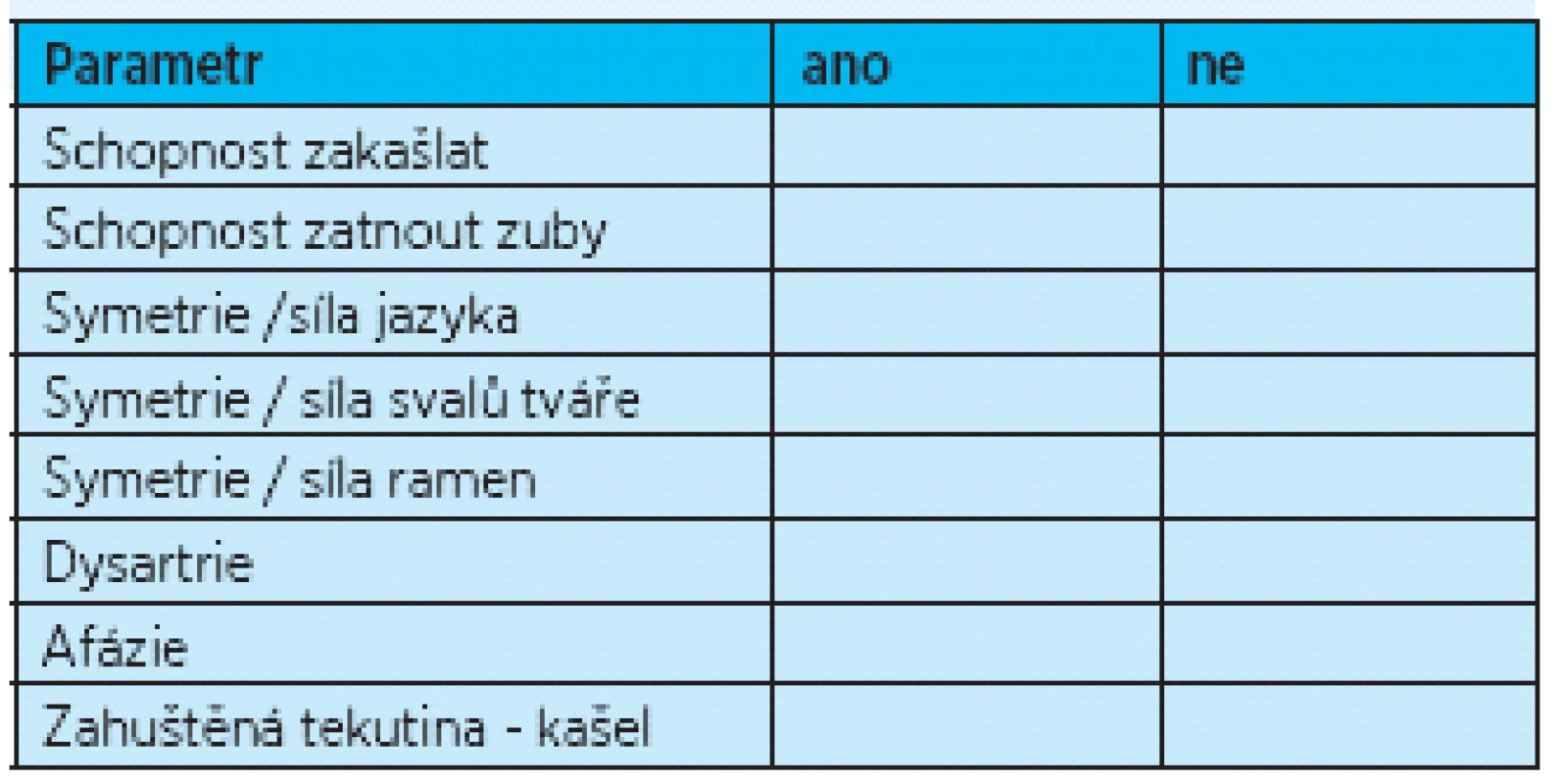
Dalším bed-side testem zjišťujícím schopnost polykání je Gugging Swallowing Screen (GUSS) (11), který po úvodním nepřímém testu polykání testuje postupně tři konzistence stravy, počíná s podáváním tekutiny zahuštěné na konzistenci pudinku. Pokud je polykání tohoto vzorku stravy bez poruchy, pokračuje se s podáním postupně stoupajícího množství tekutiny (3, 5, 10, 20 a 50 ml). Opět pokud není shledána porucha, pokračuje test podáním tuhého sousta (suchý chléb). Na základě bodového zhodnocení test rozlišuje 4 stupně postižení s doporučením dalšího postupu vyšetření a doporučením ohledně úpravy příjmu stravy a tekutin. Senzitivita testu je 100% pro přítomnost aspirací, specificita nástroje je 50 – 60 %.
Postup péče o pacienta s poruchou polykání
Výsledkem základního vyšetření je rozhodnutí, jak upravovat dietu a rozhodnutí o potřebě provádět specializovaná instrumentální vyšetření – videoendoskopické vyšetření (FEES) nebo videofluoroskopii (VFSS).
Pacienti s poruchou polykání tvoří etiologicky rozmanitou skupinu. Kromě stanovení základní diagnózy a kauzálního řešení, pokud je to možné, je základem postupu stanovení bezpečnosti perorálního příjmu. Pokud není bezpečný perorální příjem, je nutné rozhodnutí o způsobu výživy nonorální cestou (nazogastrická sonda, perkutánní endoskopická gastrostomie, parenterální výživa)(21).
Pacient s aspirací nebo pacient, kterému polknutí bolusu stravy trvá déle než 10 sekund, je kandidátem některé formy parenterální výživy. Je-li očekáváno rychlé zlepšení, je metodou volby tenká nazogastrická sonda. Při prognóze delšího trvání poruchy polykání je vhodnější využití perkutánní endoskopické gastrostomie(13).
Využití různých forem umělé výživy v zařízeních dlouhodobé péče bylo sledováno v rámci projektu SHELTER Study (Services and Health for Elderly in Long TERm care) v 7 zemích Evropské unie (Česká republika, Finsko, Francie, Německo, Itálie, Holandsko, Velká Británie) a v Izraeli. Sledováno bylo 4156 rezidentů zařízení dlouhodobé péče v 59 zařízeních. V České republice bylo sledováno 500 klientů v 10 zařízeních, za použití dotazníkového nástroje „inter RAI – Long Term Care Facility Instrument“. Výživa pomocí sondy byla využívána u 3,3 % klientů (0,65 % nazogastrická/nazojejunální sonda, 2,0 % gastrostomie, 0,65 % kombinace orální a sondové výživy). Parenterální výživa byla podávána 0,3 % klientů. Užití umělé výživy v České republice bylo srovnatelné s četností v Německu, Holandsku a Velké Británii (tab. 4, graf 1)(14).
Tab. 4. Enterální a parenterální umělá výživa v zařízeních dlouhodobé péče v zemích zúčastněných v projektu SHELTER Study 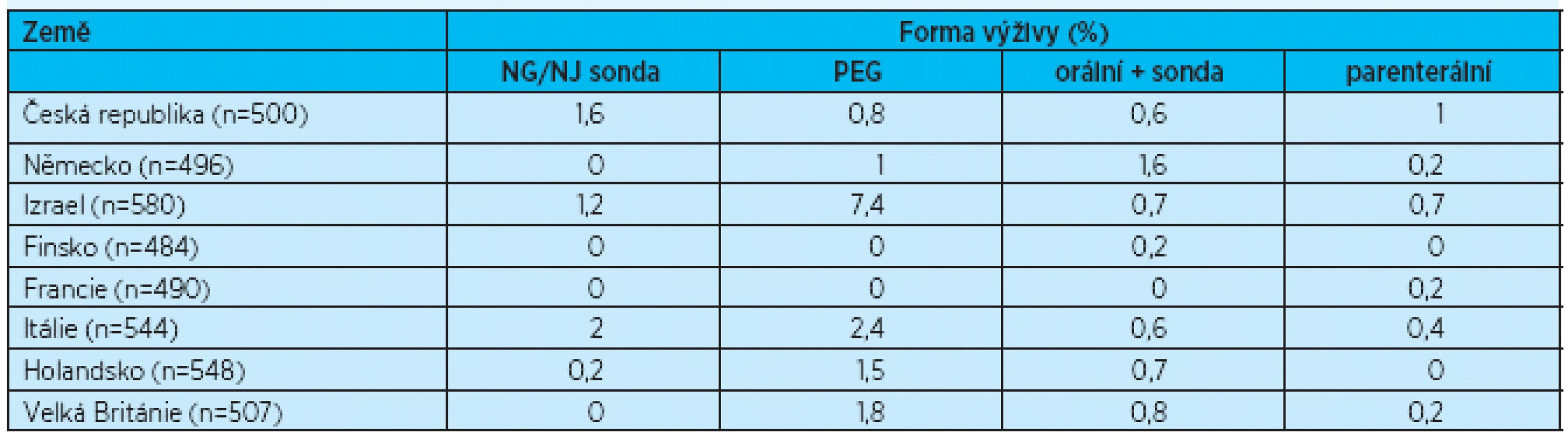
Graf 1. Použití nonorální výživy u rezidentů dlouhodobé péče v zemích zúčastněných v projektu SHELTER 
Problematickým je rozhodování o sondové výživě u pacientů nespolupracujících a pacientů s těžkou demencí. Ve studii Kuo et al. (2009) bylo zjištěno, že roční mortalita pacientů se zavedenou sondovou výživou u dysfagie při pokročilé demencí dosahovala 64,1 % , medián přežití byl 56 dnů od zavedení sondy(24).. Obdobnou roční mortalitu 63% pacientů se zavedenou PEG uvádí studie Grant et al. (1998)(25).
V kampani, pořádané ve spolupráci Americké geriatrické společnosti a Americké internistické společnosti, „Vybírejte moudře: pět věcí, které by lékaři a pacienti měli zvažovat“ je jako první bod uvedeno nedoporučovat zavedení PEG u pacientů s pokročilou demencí. Místo PEG a artificiální nutrice se preferuje krmení pacienta vhodně upravenou stravou(26).
Pokud je možný alespoň částečný perorální příjem, je možné využít kompenzačních strategií, které zahrnují techniku držení těla, posílení senzorických podnětů, změnu konzistence stravy, modifikaci objemu a rychlosti příjmu stravy.
Pacient s dysfagií často není schopen adekvátního příjmu stravy a tekutin, sledování hydratace a nutričního stavu pacientů je jedním ze základních postupů. Pro sledování nutričního rizika geriatrických pacientů je nejvíce doporučován dotazník Mini Nutritional Assessment (MNA)(27).
Součástí péče o pacienta s dysfagií je rehabilitační péče využívající cviků k posílení svalů zúčastněných na perorálním příjmu. Nácvik polykání bez bolusu potravy je označovaný jako nepřímá léčba, nácvik polykání sousta je označovaný jako přímá léčba poruch polykání. Rehabilitaci je možné provádět i u pacientů se zavedenou nazogastrickou sondu nebo perkutánní gastrostomií(2). Intervence založené na nácviku polykání jsou prokazatelně účinné, zlepšují průběh polykacího aktu a snižují výskyt komplikací spojených s dysfagií (tab. 5)(18, 19, 20).
Tab. 5. Zjednodušený algoritmus managementu péče o pacienta s poruchou polykání 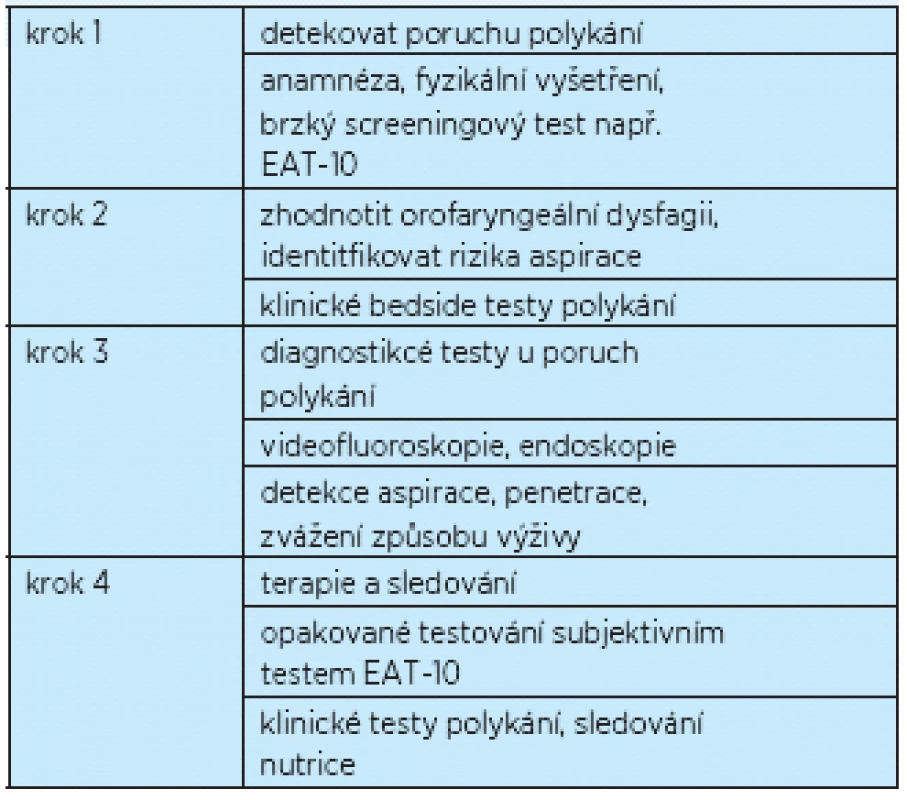
Závěr
Poruchy polykání jsou častým a závažných problémem postihujícím významné množství geriatrických pacientů. Identifikaci a časnému záchytu těchto obtíží je potřeba věnovat náležitou pozornost. Vzhledem k širokému spektru onemocnění vedoucích k dysfagii není možné použít žádný z objektivizujících testů univerzálně. Je vytvořeno několik dotazníkových nástrojů pro posouzení polykacích obtíží.
Subjektivní dotazníkový nástroj EAT-10 dokáže detekovat širší oblast poruch polykání již v počátečních fázích obtíží, je jednoduše proveditelný a časově nenáročný, jeho zavedení do širší praxe může pomoci zaměřit pozornost na zatím často opomíjenou oblast poruch polykání a tím předejít závažným zdravotním komplikacím vyplývajícím z malnutrice a následků aspirací. Jde o dotazník vhodný i pro samostatné vyplnění pacientem, lze ho v širší míře využívat v ambulantní péči.
Ostatní uváděné testy jsou určeny primárně pro sledování polykání u pacientů po cévních mozkových příhodách. Jedná se o klinické bed-side testy prováděné zdravotnickým pracovníkem, zaměřují se především na závažné projevy penetrace a aspirace.
Včasná detekce dysfagie a doporučení vhodné formy a úpravy stravy je zásadním prvkem v péči o pacienty s postižením polykacího aktu.
MUDr. Pavlína Malochová,
MUDr. Pavla Mádlová,
MUDr. Tomáš Richter,
prof. MUDr. Eva Topinková, CSc.
Geriatrická klinika 1. LF UK a VFN, Praha
MUDr. Pavlína Malochová
e-mail: pavlina.malochova@vfn.cz
Promovala na 1. lékařské fakultě UK v Praze. Od roku 2004 pracuje na Geriatrické klinice VFN, kde v roce 2013 složila atestaci z geriatrie.
Zdroje
1. Kawashima K, Motohashi Y, Fujishima: Prevalence of dysfagia among community-dwelling elderly individuals as estimated using a questionnaire for dysphagia screening. Dyphagia 2004; 19(4): 266–271.
2. Tedla M, Komínek P, Chrobok V et al.: Poruchy polykání. 1. vyd. Tobiáš, Havlíčkův Brod 2009.
3. Jurašková B, Hrnčiariková D, Holmerová I et al..: Poruchy výživy ve stáří. Medicína pro praxi 2007; 4(11): 443–446. www:solen.cz/pdf/med/2007/11/02.pdf
4. Masiero S, Piebon R, Previato C, Gomero E: Pneumonia in stroke patients with oropharyngeal dysphagia: a six month follow up study. Neurol Sci 2008; 29 : 139–145.
5. Karásková L, Škvrňáková J, Mandysová P: Zjišťování subjektivních změn v polykání u seniorů. Geri a gero 2012; 1 : 20–23.
6. Belafsky PC, Mouadeb DA, Rees CJ et al.: Validity and reliability of eating assesment tool (EAT-10). Annals of Otology, Rhinology and Laryngology 2008; 117(12): 919–924.
7. Mandysová P, Petržílková K, Škvrňáková J, Karásková L: Subjektivně pociťované potíže s polykáním – využití nástroje EAT-10. Česká a Slovenská neurologie a neurochirurgie 2011; 74(107): 118–119.
8. Daniels SK, Brailey K, Priestly DH et al.: Aspiration in patients with acute stroke. Arch Phys Med Rehabil 1998; 79(1): 14–9.
9. Daniels SK, Ballo LA, Mahoney MC, Foundas AL: Clinical predictors of dysphagia and aspiration risk: outcome measures in acute stroke patients. Arch Phys Rehabil 2000; 81 : 1030-1033.
10. Mandysová P, Ehler E, Škvrňáková J a kol.: The development of an eight-item test for nurse-led dysphagia screen. Ošetrovateĺstvo: teória, výskum, vzdelávanie (online) 2012; 2(2): 45–50. www.osetrovatelstvo.eu
11. Trapl M a kol.: Dysphagia Bedside Screening for Acute-stroke Patients. Stroke. Ahajournals. org/content/38/11/2948.full
12. Rosenbeck JC, Robbins J, Roecker EB et al.: Penetration-Aspiration Scale. Dysphagia 1996; 11 : 93–8.
13. Logemann JA: Evaluation and Treatment of Swallowing Disorders, second edition, Austin: PROED 1998; 53–54.
14. Onder G, Carpenter I, Finne-Soveri H et al.: Assessment of nursing home residents in Europe: the Services and Health for elderly in Long TERm care ( SHELTER) study, BMC Health Serv Res 2012; 12 : 5.
15. Carnaby G, Hankey GJ, Pizzi J.: Behavioral intervention for dysphagia in acute stroke: a randomised controlled trial. Lancet Neurol 2006; 5 : 31–37.
16. Logemann JA, Gensler G, Robbins J, et al.: A randomized study of three interventions for aspiration of thin liquids in patiens with dementia or Parkinson’s disease. J Speech Lang Hear Res 2008; 51 : 173–183.
17. Groher ME, Crary MA: Dysphagia: clinical management in adults and children. maryland heights. MO: Mosby Elsevier 2010.
18. Kahrilas PJ, Logemann JA, Krugler C, Flanagan E: Volitional augmentation of upper aesophageal sphincter mening during swallowing. AM J Physiol 1991; 260 : 450–456.
19. Sura L, Madhavan A, Carnaby G, Crary M: Dysphagia in the elderly: management and nutritional considerations. Clinical Interventions in Aging 2012; 7 : 287–298.
20. Carnaby G, Hankey GJ, Pizzi J: Behavioral intervention for dysphagia in acute stroke: a randomised controlled trial. Lancet Neurol 2006; 5 : 31–37.
21. Topinková E: Geriatrie pro praxi. Praha, Galén 2005.
22. Shaker R, Easterling C, Kern M et al.: Rehabilitation of swallowing by exercise in tube fed patiens with pharyngeal dysphagia secondary to abnormal UES mening. Gastroenterology 2002; 122 : 1314–1321.
23. Shaker R, Kern M, Bardan E et al.: Augmentation of deglutitive upper esophageal sphincter mening in elderly by exercise. AM J Physiol 1997; 272 : 1518–1522.
24. Kuo S, Rhodes RL, Mitchell SL et al.: Natural history of feeding-tube use in nursing home residents with advanced dementia. J Am Med Dir Assoc 2009; 10(4): 264–270.
25. Grant MD, Rudberg MA, Brody JA: Gastrostomy placement and mortality among hospitalized Medicare beneficiaries. JAMA 1998; 279 : 1973–1976.
26. http://www.americangeriatrics.org/healthcare proffessionals/practice management/choosing wisely
27. Topinková E: Využití standardizovaných škál pro hodnocení stavu výživy u starších nemocných. Čes Geriatr Rev 2003; 11 : 6–11.
Štítky
Geriatria a gerontológia Praktické lekárstvo pre dospelých Protetika
Článok vyšiel v časopiseGeriatrie a Gerontologie
Najčítanejšie tento týždeň
2013 Číslo 3- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Vareniklin jako pomocník v léčbě nikotinismu i u psychiatrických pacientů
-
Všetky články tohto čísla
- Certifikace Vážka – zkušenosti a reflexe
- Gerontologická a organizační supervize – odborná podpora a organizační supervize v zařízeních pro seniory zřizovaných Jihomoravským krajem (GOS)
- Dny paměti 2008–2012. Výsledky pěti let testování paměti v ČR
- Prevalence kognitivních poruch v pobytových zařízeních pro seniory v ČR - nárůst mezi lety 2007 a 2013
- Vplyv fyzioterapiena sebestačnosť geriatrických pacientov
- Jaká je kapacita a struktura dlouhodobé péče v České republice?
- Aktivní stárnutí v obcích ČR
- Problematika hodnocení tělesné způsobilosti u seniorské populace
- Funkční hodnocení seniorů, teorie a praxe
- Využití Mezinárodní klasifikace funkčních poruch, disability a zdraví – ADL a IADL v posuzování stupně závislosti
- Staging u neurodegenerativních demencí
- Ergoterapie v péči o pacienty s demencí a na geriatrickém pracovišti
- Význam podpůrné (svépomocné) skupiny pro rodinné pečující o seniora se syndromem demence
- Plány Alzheimer – potřeba, nutnost nebo zbytečný přepych?
-
Strategie České alzheimerovské společnosti P-PA-IA
Péče a podpora lidem postiženým syndromem demence -
Dokážeme včasně diagnostikovat poruchy polykání?
Časný screening poruch polykání, kazuistiky - Geriatrické drobnosti – tři kazuistiky
- Geriatr a tzv. „sociální“ zařízení
- Sociální práce na geriatrickém pracovišti
- Role klinického farmaceuta v geriatrické péči
- Význam geriatrické medicíny nejen v dlouhodobé péči
- Jubilující Eva Topinková
- Životní jubileum Iva Bureše
- Editorial
- Geriatrie a Gerontologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Vplyv fyzioterapiena sebestačnosť geriatrických pacientov
- Geriatrické drobnosti – tři kazuistiky
-
Dokážeme včasně diagnostikovat poruchy polykání?
Časný screening poruch polykání, kazuistiky - Ergoterapie v péči o pacienty s demencí a na geriatrickém pracovišti
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy