8. Aplikace kyslíku v resuscitaci na porodním sále – doporučený postup
Autoři:
J. Dort; E. Dortová
Vyšlo v časopise:
Ceska Gynekol 2013; 78(Supplementum): 89-91
Kategorie:
DOPORUČENÉ POSTUPY
ČESKÉ NEONATOLOGICKÉ SPOLEČNOSTI
Autoři
J. Dort, E. Dortová
Oponenti
Výbor České neonatologické společnosti ČLS JEP
I. Úvod, definice problému a cíl
Kyslík je na světě nejčastější lék podávaný novorozencům, přesto se hodnoty optimální oxygenace u novorozence stále hledají.
Oxygenace tkání závisí na:
- perfuzi,
- Hb,
- saturaci Hb kyslíkem.
Arteriální krevní tlak není spolehlivým ukazatelem kvality perfuze tkání. Ta kromě krevního tlaku závisí na srdečním výdeji, cirkulujícím volumu, stavu periferního řečiště.
Disociační křivka fetálního Hb je posunuta doleva, a proto může být dostatečná SpO2 Hb a oxygenace tkáně dosažena i při relativně nízkém PaO2. Optimální oxémie pro nezralé děti a jí odpovídající SpO2 se intenzivně hledá.
Vzduch samotný ve srovnání s intrauterinním prostředím představuje již hyperoxické prostředí. Normální SpO2 in utero je 0,50–0,60, za patologickou je považována až nižší než 0,30.
Měření oxygenace
paO2
Vyjadřuje aktuální hodnotu v arteriální/arterializované krvi v okamžiku odběru, získanou v rámci měření acidobazické rovnováhy.
U donošených novorozenců je paO2 10–12 kPa (75 až 90 mm Hg).
U nedonošených dětí z obavy z poškození plic a vzniku retinopatie se mohou používat hodnoty i nižší, při nichž je zachován aerobní metabolismus.
TcpO2
Málo spolehlivé, transkutánní oxymetry vyžadují časté kalibrace, mohou způsobit popálení kůže.
SpO2
Je přímo úměrná pO2 (ve střední části disociační křivky), pulzní oxymetry měří kontinuálně bez potřeby kalibrace, jsou dostatečně citlivé pro detekci hypoxémie.
SpO2 ale nemusí vypovídat o tkáňové oxygenaci, při vysokých hodnotách blížících se 100 % se snižuje přesnost, není vhodná k průkazu hyperoxémie (tu odhalí pouze paO2)!!!
K měření SpO2 se užívají v současnosti monitory vybavené SET systémem (Signal Extraction Technology), které odliší karboxyhemoglobin, methemoglobin a venózní hemoglobin a snímají pouze arteriální signál. To je velmi důležité, protože příměs venózního signálu může totiž vést k měření falešně nízké hodnoty SpO2.
Volné kyslíkové radikály a poškození tkání a orgánů
Vznikají při aerobním metabolismu. Za fyziologických podmínek jsou v mitochondriích asi 2 % spotřebovaného kyslíku redukována na superoxidový radikál, který se uplatňuje v různých buněčných funkcích. Buňky jsou vybaveny schopností udržovat redoxní stabilitu. K obraně slouží superoxidismutáza a kataláza (u novorozenců snížená aktivita), vitamin E, bilirubin, transferin (také laktoferin MM).
Hyperoxie, ale i různé další vlivy mohou spustit nadprodukci kyslíkových radikálů, ty změní permeabilitu mitochondriálních membrán, ze kterých se uvolní cytochrom c a další faktory apoptózy, je alterována např. syntéza proteinů, buněčný růst, vznikají zlomy DNA a nastává smrt buněk. Nadbytek volných kyslíkových radikálů je pro buňky škodlivý, způsobuje stárnutí, poškození DNA, neoplazmata, retinopatii nedonošených novorozenců (ROP), bronchopulmonální dysplazii.
ROP je nejčastější příčina poruchy zraku či slepoty u dětí na světě. V etiologii se významně uplatňuje hyperoxie, následující vazokonstrikce vyvolává ischémie nezralé sítnice, pak stimulaci endoteliálního růstového faktoru (VEGF) a výsledkem je patologická proliferace cév. BPD má multifaktoriální etiologii, v níž hyperoxie je opět také důležitý faktor.
Byla vyslovena hypotéza, že ROP, BPD, PDA, IVH a NEC by mohly být různé orgánové projevy jednoho identického patofyziologického procesu, pojmenovaného neonatal oxygen radical disease [8].
Resuscitace a kyslík na porodním sále
Resuscitace s užitím kyslíku neprokázala lepší výsledky proti samotnému vzduchu. Naopak, studie ukázaly, že po-užití 100% kyslíku prodlužuje dobu nutné resuscitace! Kyslík ve vysoké koncentraci působí takový oxidativní stres, že ještě po 4 týdnech od jeho aplikace byly dokázány orgánové změny (myokardiální a renální) [10].
Použití 100 % kyslíku se ukázalo být nebezpečné, může dokonce zvyšovat mortalitu a riziko pozdních následků. Naopak při restriktivní oxygenoterapii (tj. SpO2 udržována v mezích 80–90 % ) u dětí s gestačním věkem nižším než 28 týdnů nebyly zjištěny žádné nevýhody z hlediska psychomotorického vývoje (Tin 2001).
Cíl
Stanovení pravidel pro bezpečné použití kyslíku v resuscitaci novorozence s ohledem na současné vědecké poznatky o toxicitě kyslíku. Otázka tedy nezní, zda v resuscitaci používat 100% nebo 21% FiO2, ale jak zajistit normoxemickou oxygenaci.
II. Použití oxygenoterapie v resuscitaci novorozencena porodním sále
Použití kyslíku musí být vždy indikované, a to rizikem hypoxického poškození.
Podávání kyslíku se nemá zahajovat dříve než po zabezpečení průchodnosti dýchacích cest, dýchání a cirkulace.
Novorozenec po porodu nemusí být ihned růžový!
Zahájení resuscitace primárně vzduchem.
Postup resuscitace
1. minuta
Zdroj tepla
Osušení
Polohování a odsátí dýchacích cest
Zhodnocení stavu
Stimulace dýchání
Prodýchání vakem přes masku – vzduchem
2. minuta
Zhodnocení stavu opakovaně
Pokračování dýchání vakem přes masku – vzduchem
Nepřímá masáž srdeční
PULZNÍ OXYMETRIE – senzor na pravou ruku (krátce po narození je preduktální oxygenace lepší).
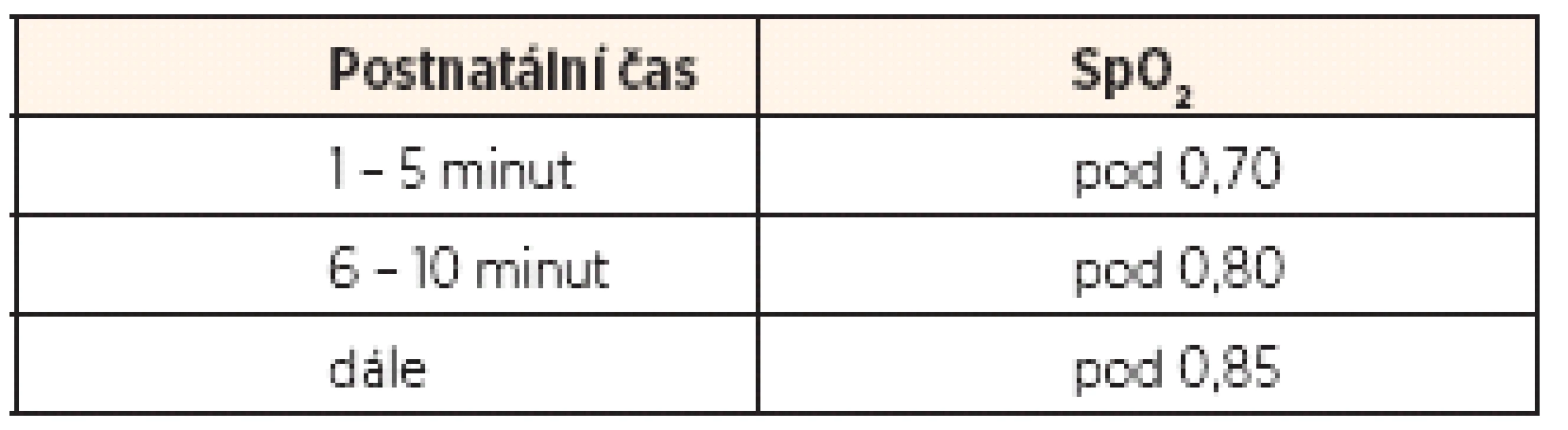
3. minuta
OXYGENOTERAPIE
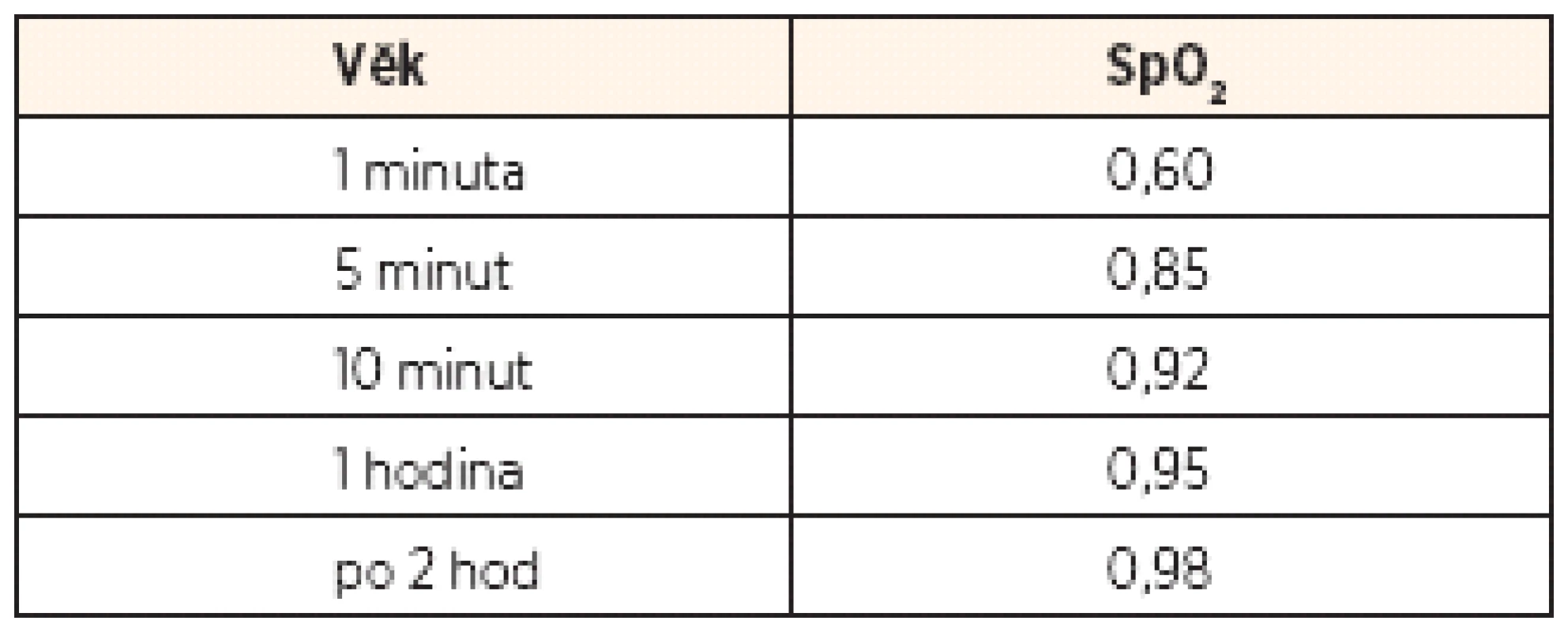
Indikovaně podle stavu dítěte a SpO2. Rozhodující jeaktuální hodnota SpO2 v daném čase po přerušení pupečníku.
4. minuta a dále
Standardní postup resuscitace.
III. Souhrn zásad oxygenoterapie
Nepřiměřené použití kyslíku u novorozence přináší riziko závažného orgánového a tkáňového poškození:
- retinopatie nedonošených,
- bronchopulmonální dysplazie,
- postižení vyvíjejícího se mozku,
- infekce,
- poškození DNA a riziko malignity později.
Prevence hypoxického postižení (například po asfyxii) je nutná, ale současně je nutné vyhnout se hyperoxémii.
Dávkování kyslíku musí být individuální k zajištění normoxemické oxygenace. K tomu je třeba používat spolehlivé monitory ihned od narození, podávat oxygenoterapii podle aktuálních hodnot SpO2 a dodržovat doporučené limity SpO2, které byly potvrzeny jako bezpečné z hlediska nejen krátkodobého, ale také dlouhodobého výsledku (podle psychomotorického vývoje).
Zkratky
BPD – bronchopulmonální dysplazie
GV – gestační věk
FiO2 – akce kyslíku ve vdechované směsi
IVH – intraventrikulární krvácení
NEC – nekrotizující enterokolitida
NNPH – novorozenec s nízkou porodní hmotností
NVNPH – novorozenec s velmi nízkou porodní hmotností
NENPH – novorozenec s extrémně nízkou porodníhmotností
paO2 – parciální tlak kyslíku v arteriální krvi
PDA – otevřená tepenná dučej
PS – porodní sál
ROP – retinopatie nedonošených
SpO2 – saturace hemoglobinu kyslíkem
TcpO2 – transkutánně měřený parciální tlak kyslíku v krvi
Poznámka
Toto doporučení nepostihuje a ani nemůže postihnout všechny alternativy, které mohou v klinické praxi nastat. Pro naprostou většinu klinických situací však představuje tento doporučený postup návod, jak snížit riziko hypoxie a na druhé straně snížit riziko projevů kyslíkové toxicity.
Zdroje
1. Bancalari, E. Changes in the pathogenesis and prevention of chronic lung disease of prematurity. Am J Perinatol, 2001, 18, p. 1–9.
2. Deulofeut, R., Critz, A. Avoiding hyperoxia in infants under 1250g is associated with improved short- and long-term outcomes. J Perinatol 2006, 26, p. 700–705.
3. Deulofeut R., Sola A. Risk for late bacterial sepsis in infants under 1000g: another beneficial effect of avoiding hyperoxia?E- PAS 2006, 59, p. 148.
4. International Liaison Committee on Resuscitation. Part 7: Neonatal resuscitation. Resuscitation, 2005, 67, p. 293–303.
5. Kabon B., Kurz A. Optimal perioperative oxygen administration. Curr Opin Anesthesiol, 2006, 19, p. 11–18.
6. Naumburg E., Bellocco R., Cattingius S., et al. Supplementary oxygen and risk of childhood lymphatic leukaemia. Acta Paediatr, 2002, 91, p. 1328–1333.
7. Richmond S., Goldsmith JP. Refining the role of oxygen administration during delivery room resuscitation: What are the future goals? Semin Fetal Neonatal Med, 2008, 13, 6, p. 368–374.
8. Saugstad OD., Rootwelt T., Aalen O. Resuscitation of asphyxiated newborn infants with room air or oxygen: an international controlled trial: the Resair 2 study. Pediatrics, 1998, 102.
9. Saugstad OD. Resuscitation of newborn infants with room air or O2. Semin Neonatol, 2001, 6, p. 233–239.
10. Saugstad OD. Oxygen toxicity at birth: the pieces are put together. Pediatr Res, 2003, 54, p. 789.
11. Saugstad OD. Optimal oxygen therapy in the newborn period. Pediatric Pulmonol, 2004, S26, p. 112–113.
12. Saugstad OD. Resuscitation with pure oxygen at birth: it is time for a change. J Matern Fetal Neonatal Med, 2004, 15, p. 73–74.
13. Schmidt RF. Memorix- Fyziologie, p. 213–216.
14. Sola A. Oxygen as a neonatal health hazard, p. call for détente in clinical practics Review article, Dallas, Acta Paediatrica June, 2007, 96, 6, p. 801–812.
15. Sola A. Prevention of retinopathy of prematurity European Academy of Pediatrics, Barcelona, October 7.–10. 2006, p. 64.
16. Spector LG., Klebanoff MA., Feusner JH., et al. Childhood cancer following neonatal oxygen supplementation. J Pediatr, 2005, 147, p. 27–31.
17. Rowland R., Newman CGH. Pulmonary complications of O2 therapy. J Clin Path, 1969, 22, p. 192–198.
18. Zoban P., Biolek J. Léčba kyslíkem. Doporučené postupy ČNeoS, 2007.
19. Morley JM., Davis PG. Advances in neonatal resuscitation, p. supporting transition. Arch Dis Child Fetal Neonatal Ed, 2008, 93,5, p. F334–336.
Štítky
Detská gynekológia Gynekológia a pôrodníctvo Reprodukčná medicínaČlánok vyšiel v časopise
Česká gynekologie

2013 Číslo Supplementum
- Ne každé mimoděložní těhotenství musí končit salpingektomií
- Mýty a fakta ohledně doporučení v těhotenství
- Je „freeze-all“ pro všechny? Odborníci na fertilitu diskutovali na virtuálním summitu
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
Najčítanejšie v tomto čísle
- 19. Tokolýza – doporučený postup
- 2. Hyperbilirubinémie novorozence – doporučený postup
- 30. Dystokie ramének – doporučený postup
- 4. Současné názory na management odtoku plodové vody
