-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Hodnocení slizničního hojení v průběhu biologické léčby Crohnovy choroby tenkého střeva pomocí kapslové endoskopie: prospektivní observační studie
Assessment of mucosal healing during biological therapy of small bowel Crohn’s disease by capsule endoscopy: a prospective observational study
Background:
Efficacy of anti-TNFα therapy in mucosal healing of Crohn’s disease in the small bowel is examined less than in the large bowel due to more difficult detection of mucosal changes.Aim and methods:
The aim of the prospective study was to assess the efficacy of anti-TNFα therapy in mucosal healing of small bowel CD using capsule endoscopy (CE). Patients with CD involving small (+/ - large) bowel, who were indicated to anti-TNFα therapy were included.Results:
25 patients (18 treated with infliximab, 7 with adalimumab) were examined by CE (Mirocam(R), IntroMedic, South Korea) at the start of biologic treatment and 19 of them during the maintenance phase of therapy. Mucosal inflammatory changes were assessed by the Lewis score (LS). The median LS at base line was 1,350 (range 337–7,840) with 28% having mild (LS 135–790) and 72% moderate to severe mucosal inflammation (LS > 790). A significant reduction of LS to 402.5 with the range of 0–4,432 (p < 0.001) was observed after median of 32 weeks of treatment, with 83% of patients having only mild mucosal inflammation or normal mucosal finding (LS < 135). Only one (2.3%) capsule retention was observed; other complications were not observed.Conclusion:
Anti-TNFα therapy is effective in mucosal healing of small bowel CD. Capsule endoscopy detected mucosal changes effectively, was well tolerated and relatively safe.Key words:
Crohn’s disease – small intestine – mucosal healing – capsule endoscopy
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.Submitted:
7. 2. 2013Accepted:
9. 2. 2013
Autoři: N. Machková 1; D. Ďuricová 1
; M. Bortlík 1,2; Luděk Hrdlička 1; M. Lukáš Jr. 1,2; M. Lukáš 1,3
Působiště autorů: Klinické a výzkumné centrum pro střevní záněty ISCARE a 1. LF UK Praha 1; Interní klinika 1. LF UK a ÚVN Praha 2; Ústav klinické biochemie a laboratorní diagnostiky 1. LF UK Praha 3
Vyšlo v časopise: Gastroent Hepatol 2013; 67(1): 17-21
Kategorie: IBD: původní práce
Souhrn
Úvod:
Efektivita anti-TNFα terapie v navození slizničního hojení u Crohnovy nemoci (CN) v tenkém střevě je prozkoumána méně ve srovnání s tlustým střevem z důvodu obtížnější detekce slizničních změn.Cíl a metodika:
Cílem této prospektivní studie bylo ověřit účinnost anti-TNFα léčby v dosažení slizničního hojení CN tenkého střeva s využitím kapslové endoskopie (CE). Do studie byli zařazeni pacienti s CN tenkého (+/ - tlustého) střeva, kteří byli indikováni k léčbě anti-TNFα preparáty.Výsledky:
25 pacientů (18 léčených infliximabem, 7 adalimumabem) bylo vyšetřeno CE (Mirocam®, IntroMedic, Jižní Korea) při zahájení biologické terapie a 19 z nich v průběhu udržovací fáze léčby. Nález byl hodnocen pomocí Lewisova skóre (LS). Medián celkového LS byl při vstupu do studie 1 350 (rozmezí 337–7 840), 28 % pacientů mělo lehké slizniční zánětlivé změny (LS 135–790) a 72 % mělo změny střední až těžké (LS > 790). Po léčbě v trvání (medián) 32 týdnů došlo k signifikantnímu poklesu celkového LS na 402,5 (rozmezí 0–4 432; p < 0,001), přičemž 83 % pacientů mělo pouze lehké zánětlivé změny nebo normální slizniční nález (LS < 135). V jednom případě (2,3 %) došlo k retenci kapsle, jiné komplikace nebyly pozorovány.Závěr:
Práce prokázala účinnost anti-TNFα terapie v indukci slizničního hojení CN tenkého střeva. Kapslová endoskopie byla v této situaci metodou efektivní, pacienty dobře tolerovanou a bezpečnou.Klíčová slova:
Crohnova nemoc – tenké střevo – slizniční hojení – kapslová endoskopie
Crohnova nemoc (CN) je chronické zánětlivé onemocnění, které může postihovat kteroukoli část trávicí trubice. Často vede k těžkým strukturálním změnám s rozvojem komplikací (píštěle, abscesy, stenózy) a nutností chirurgické léčby. Ve snaze zabránit nepříznivému vývoji CN se v poslední době mění strategie medikamentózní léčby, jejímž cílem je dosáhnout nejen klinické remise, ale i slizničního hojení, které je považováno za významný prognostický faktor zlepšení dlouhodobého průběhu nemoci. Efektivita anti-TNFα terapie v navození slizničního hojení u CN byla potvrzena především v tlustém střevě. Účinnost v dosažení slizničního hojení tenkého střeva je ověřena méně díky obtížnější detekci slizničních změn v této lokalizaci. Kapslová endoskopie (CE) přinesla významný pokrok v diagnostice onemocnění tenkého střeva, především v identifikaci diskrétních slizničních lézí. Potvrzení diagnózy u suspektní CN a stanovení rozsahu postižení tenkého střeva jsou hlavními indikacemi CE u CN [1–3]. Důležitou roli může mít také v identifikaci slizničního hojení po medikamentózní léčbě [4,5], počet studií popisujících přínos CE v této indikaci je však omezený [6].
Cílem našeho sledování bylo posoudit účinnost anti-TNFα terapie v navození slizničního hojení CN tenkého střeva za použití CE.
Pacienti a metody
Do této prospektivní studie byli zařazeni všichni pacienti s diagnózou aktivní CN tenkého střeva s postižením tračníku, nebo bez něj, kteří byli v klinickém centru ISCARE indikováni k léčbě anti-TNFα preparáty od června 2010 do dubna 2012. Při zahájení biologické terapie a následně v průběhu udržovací fáze bylo provedeno vyšetření CE ke zhodnocení efektu léčby na slizniční hojení. Všichni pacienti iniciálně absolvovali vyšetření CT nebo MRI enterografií k vyloučení těsné stenózy tenkého střeva (stenóza < 12 mm a/nebo prestenotická dilatace střevního lumen), která byla kontraindikací k CE. K vyšetření jsme použili endoskopickou kapsli Mirocam® jihokorejské firmy IntroMedic. Všichni pacienti zařazení do studie podepsali informovaný souhlas, práce byla provedena se souhlasem lokální etické komise.
Vyšetření CE
Pacienti byli vyšetřeni standardně po minimálně osmihodinovém lačnění a po perorální přípravě 2 litry roztoku polyethylenglykolu večer před vyšetřením [7].
Všechny záznamy CE byly hodnoceny jedním lékařem zkušeným v CE. Nález byl hodnocen pomocí Lewisova skóre (LS), což je validovaný skórovací index pro slizniční zánětlivé změny tenkého střeva [8]. Index hodnotí vzhled klků, výskyt slizničních ulcerací a střevních stenóz. Detailní hodnocení je uvedeno v tab. 1. Pro výpočet skóre je tenké střevo rozděleno do tří stejných segmentů. Celkové LS je součtem tzv. skóre stenózy (počet stenóz × ulcerace × prostupnost) a hodnoty skóre nejvíce postiženého segmentu ((vzhled klků × rozsah × distribuce) + (počet ulcerací × rozsah × velikost)). Hodnota LS < 135 odpovídá normálnímu či nesignifikantnímu nálezu, LS = 135–790 lehkým a LS > 790 středně těžkým až těžkým slizničním zánětlivým změnám.
Tab. 1. CE skórovací index pro slizniční zánětlivé změny tenkého střeva. Tab. 1. CE scoring index for small bowel mucosal inflammatory changes. 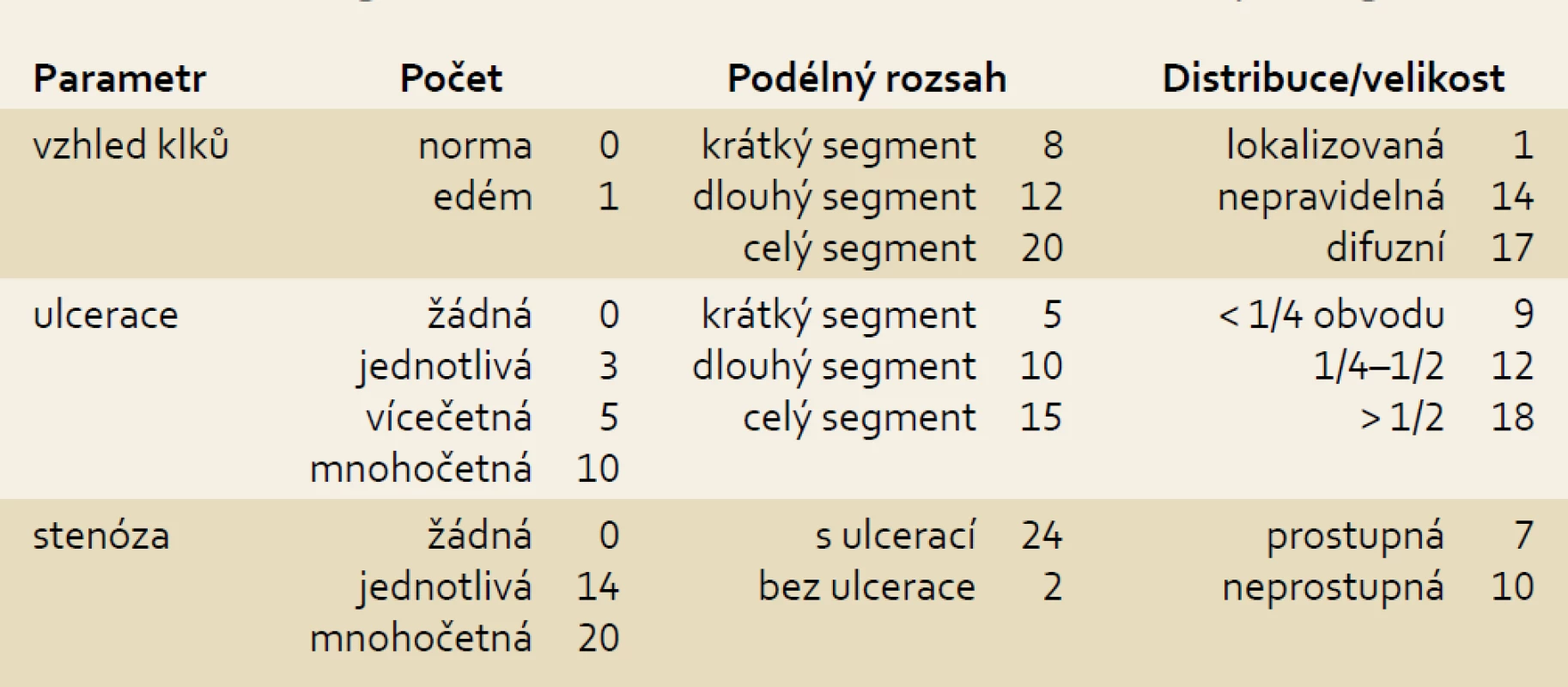
Statistická analýza
Byly použity standartní deskriptivní statistické metody zahrnující procentuální zastoupení pro kategorická data a medián (rozmezí) pro spojitá data. Výsledky LS byly analyzovány použitím Wilcoxonova párového testu s hodnotou p < 0,05 považovanou za statisticky významnou.
Výsledky
Do studie bylo zařazeno celkem 25 pacientů s CN. Základní demografická a klinická data v době prvního vyšetření CE uvádí tab. 2. 18 pacientů (72 %) bylo léčeno infliximabem (IFX) a 7 (28 %) adalimumabem (ADA). Kontrolní CE absolvovalo 19 pacientů po mediánu trvání biologické léčby 32 týdnů (rozmezí 11–55). U šesti pacientů nebyla kontrolní CE provedena z důvodu předčasného ukončení biologické léčby pro nežádoucí účinky (2), pro rozvoj stenózy na tenkém střevě (2), nespolupráci pacienta (1) a v jednom případě pro nehodnotitelný nález při nedostatečném vyprázdnění střeva. Výsledná analýza proto zahrnovala 19 pacientů, kteří absolvovali vstupní i kontrolní CE. Medián celkového LS byl při vstupu do studie 1 350 (rozmezí 337–7 840). Pět pacientů (28 %) mělo lehké slizniční zánětlivé změny (LS = 135–790) (obr. 1). Čtrnáct pacientů (72 %) mělo změny středně až těžce aktivní (LS > 790) (obr. 2 a 3). Nejčastěji byla postižena distální třetina tenkého střeva, kde byly lokalizovány i nejtěžší zánětlivé slizniční změny. Kontrolní CE po léčbě ukázala signifikantní pokles hodnoty celkového LS na medián 402,5 s rozmezím 0–4 432 (p < 0,001), přičemž 83 % pacientů mělo pouze lehké zánětlivé změny nebo normální slizniční nález (LS < 135). Kromě celkového zlepšení endoskopického nálezu byl signifikantní pokles LS pozorován i v jednotlivých segmentech střeva (tab. 3). Celkem u čtyř pacientů byla CE prokázána stenóza v průběhu tenkého střeva, jedna z nich nebyla popsána při předchozí MRI enterografii (obr. 4). Tři stenózy byly pro kapsli prostupné, v jednom případě (2,3 %) došlo k retenci kapsle ve stenóze s rozvojem subileózního stavu. Po intenzivní medikamentózní terapii (antibiotika, kortikoidy) však došlo ke spontánnímu odchodu kapsle. Jinou komplikaci jsme při CE nezaznamenali.
Tab. 2. Demografická a klinická charakteristika souboru (n = 25). Tab. 2. Demografic and clinical characteristic of the cohort (n = 25). 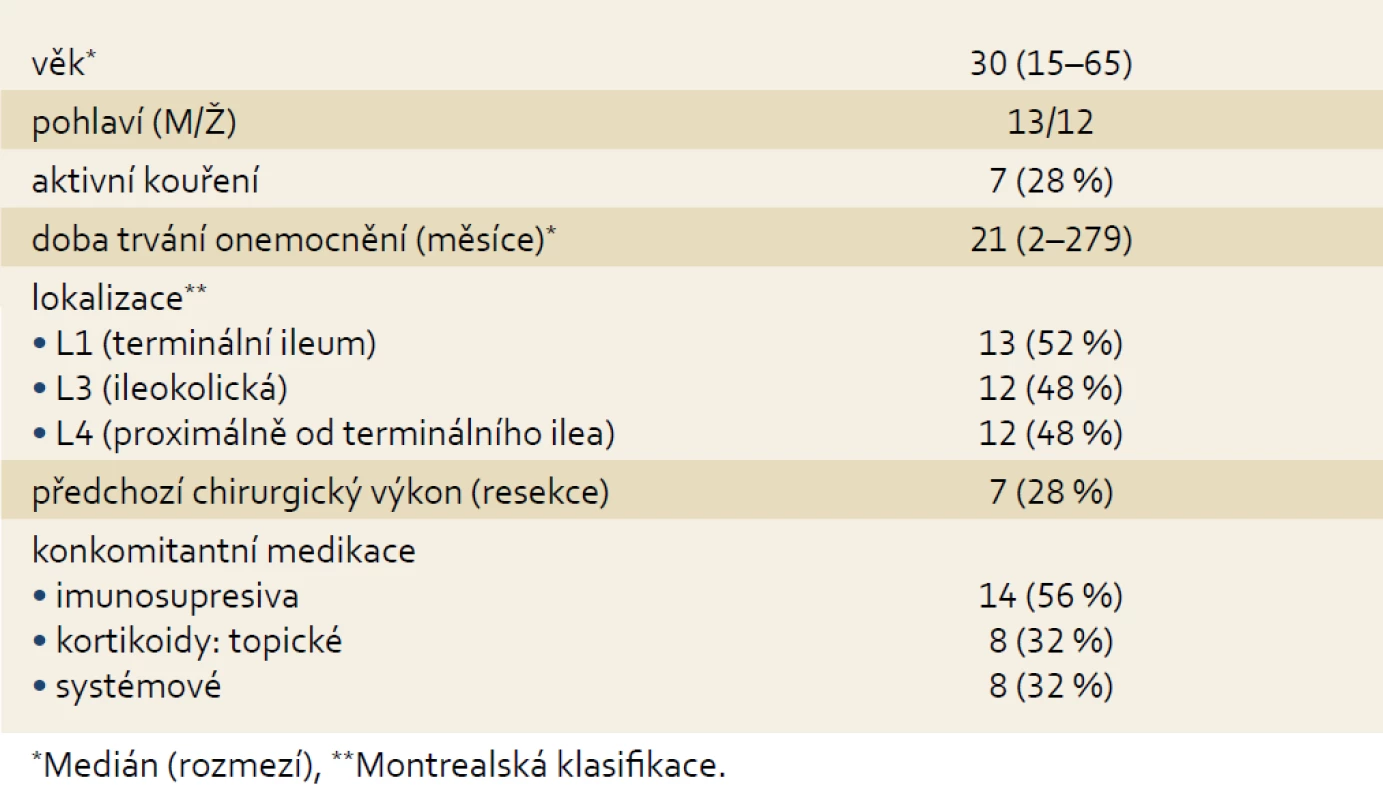
Tab. 3. Slizniční zánětlivé změny před léčbou anti-TNFα a po ní (n = 19). Tab. 3. Mucosal inflammatory changes before and after anti-TNFα therapy (n = 19). 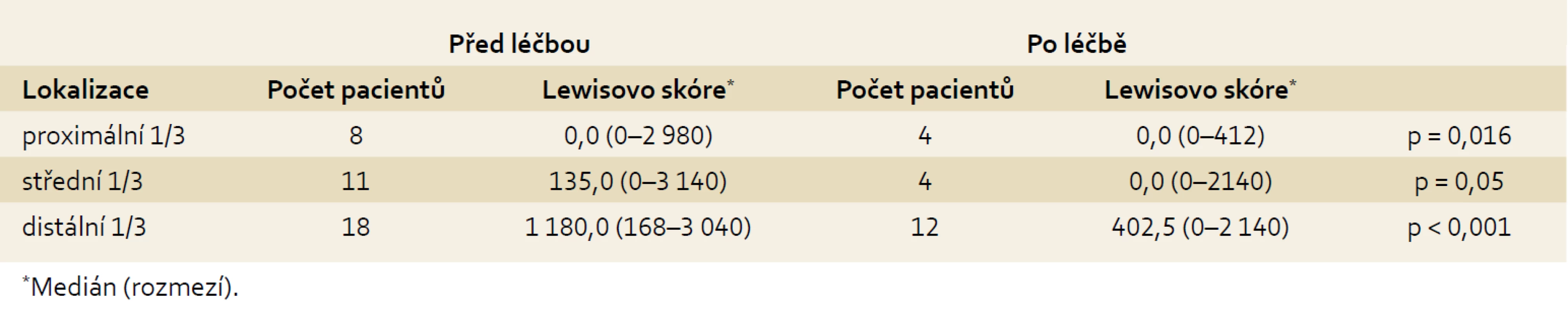
Obr. 1. Povrchové aftózní eroze v jejunu (šipky). Fig. 1. Superficial aphthous erosions in the jejunum (arrows). 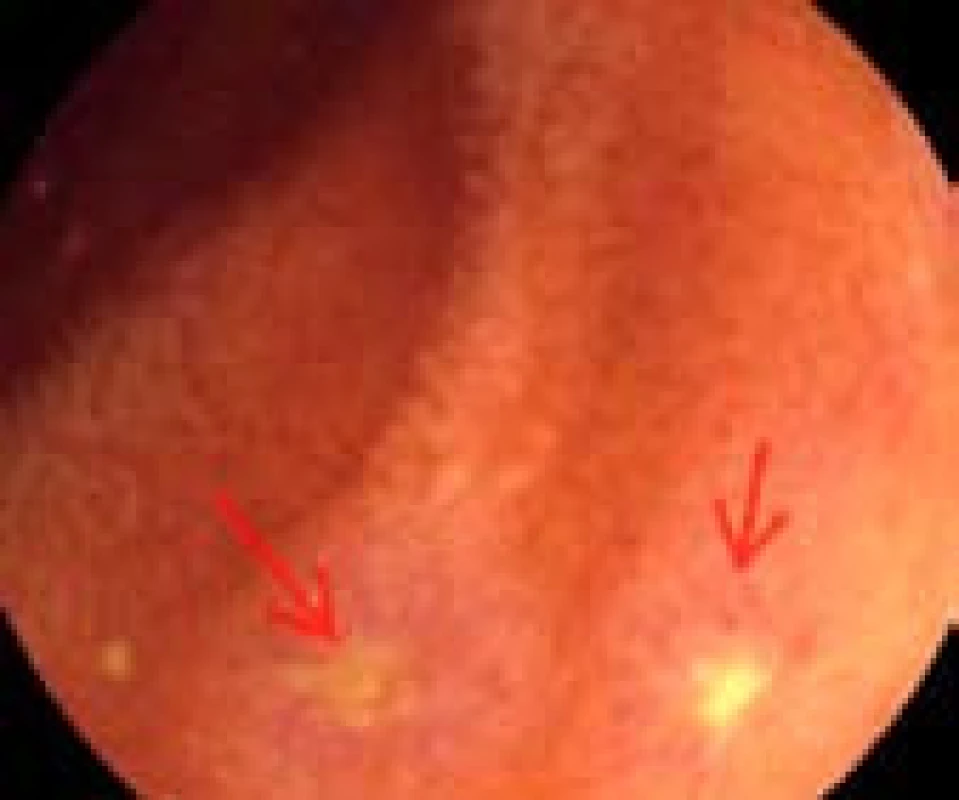
Obr. 2. Hluboká ulcerace v ileu. Fig. 2. Deep ulceration of the ileum. 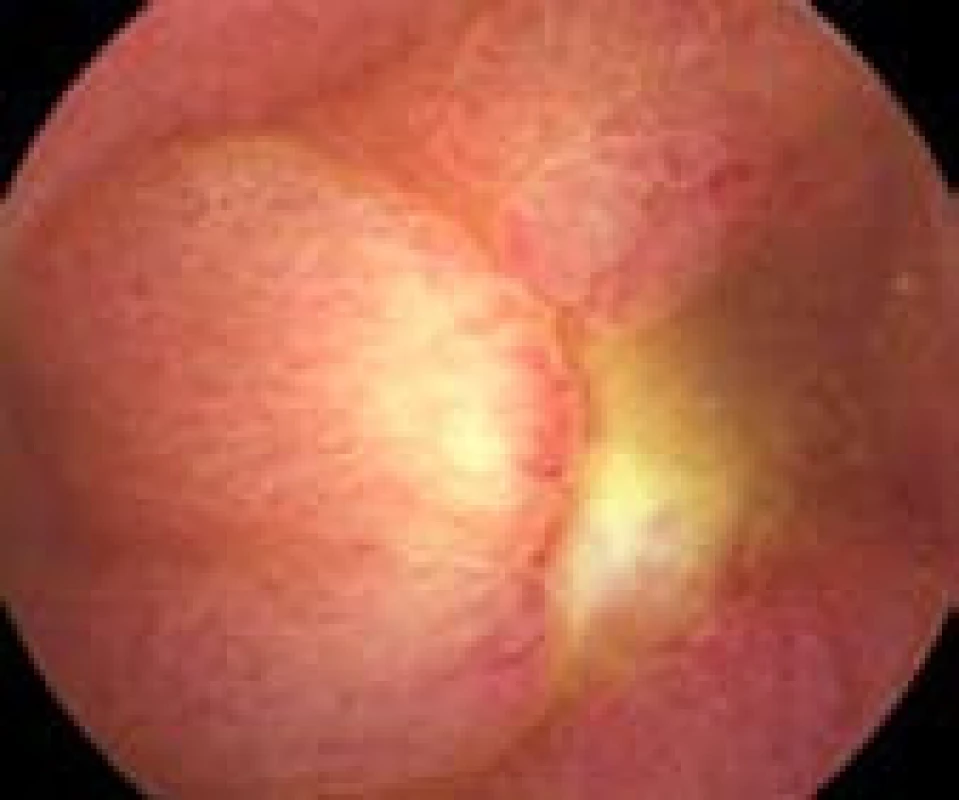
Obr. 3. Velký zánětlivý polyp v jejunu. Fig. 3. Large inflammatory polyp in the jejunum. 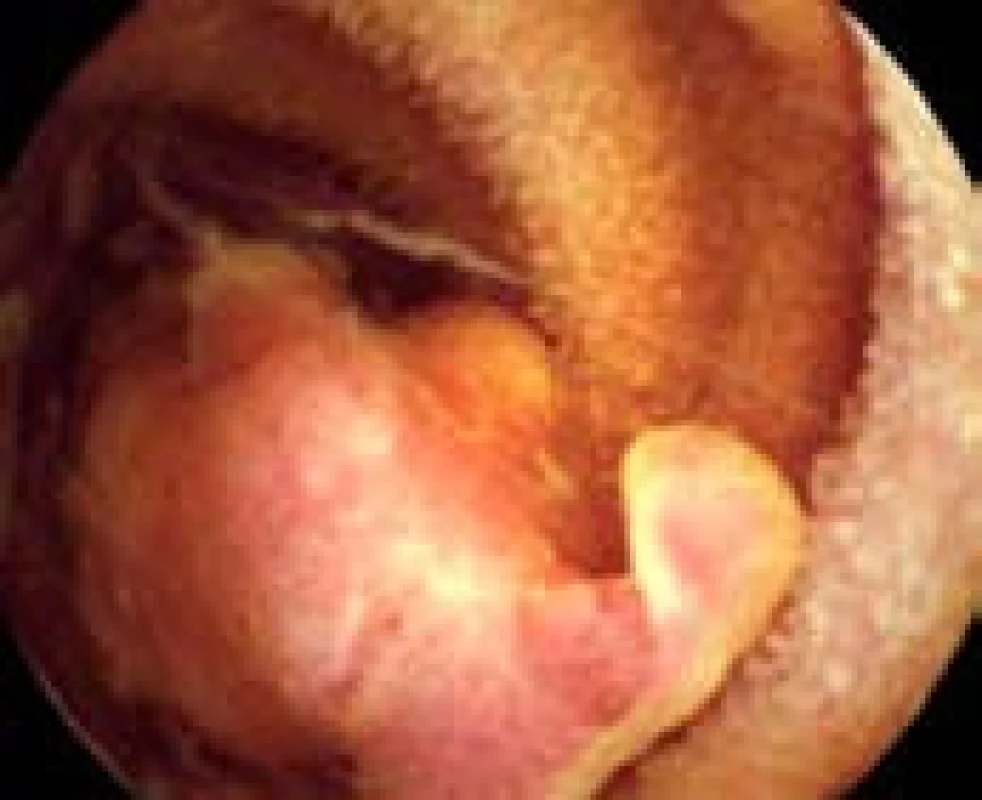
Obr. 4. Stenóza anastomózy po resekci ilea s ulcerací. Fig. 4. Stenosis of the anastomosis after ileal resection with ulcera. 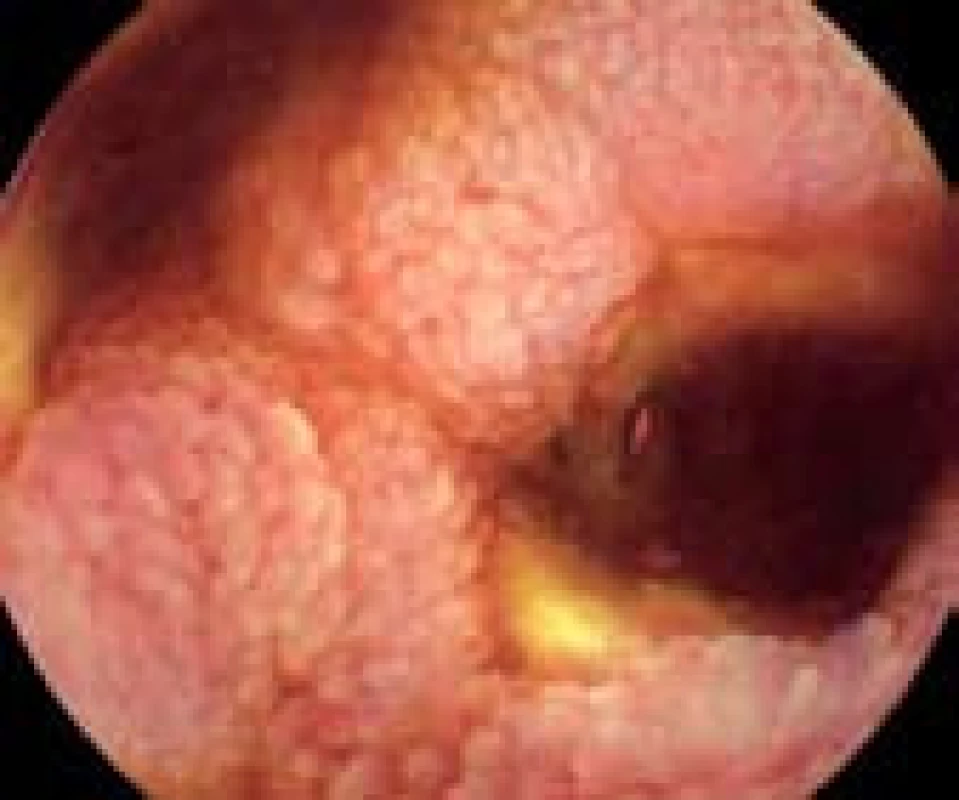
Diskuze
Práce hodnotí účinnost anti-TNFα terapie v dosažení slizničního hojení CN tenkého střeva s použitím CE. V analyzovaném souboru 19 pacientů došlo po léčbě anti-TNFα k signifikantnímu poklesu hodnoty celkového LS, a tedy k významné regresi slizničních zánětlivých změn. Indukce slizničního hojení je v současné době považována za významný prediktivní faktor zlepšení dlouhodobého průběhu CN. Populační prospektivní norská studie potvrdila, že slizniční hojení vede ke snížení těžkých strukturálních změn a je spojeno s nižším počtem komplikací a chirurgických intervencí [9]. Obdobně Baert et al prokázali, že dosažení kompletního slizničního hojení u časné CN je v průběhu následujících čtyř let spojeno se signifikantně nižší potřebou kortikoterapie [10]. Cílem medikamentózní léčby CN v současné době je dosáhnout nejen klinické remise, ale i zhojení slizničních lézí. Zásadní význam v tomto směru přinesla biologická léčba. Efektivita IFX i ADA byla prokázána výsledky velkých klinických kontrolovaných studií. Studie ACCENT1 zahrnovala endoskopickou substudii 99 pacientů, kteří byli léčeni indukční a udržovací terapií IFX nebo placebem a epizodickou léčbou IFX po dobu jednoho roku. V 54. týdnu vykazovalo 44 % pacientů léčených IFX kompletní slizniční hojení ve srovnání s 18 % léčenými placebem [11]. Účinnost IFX v indukci slizničního hojení a zlepšení dlouhodobého průběhu onemocnění s nižším počtem chirurgických výkonů (14,1 % u pacientů s kompletním slizničním hojením vs 38,4 % bez dosaženého slizničního hojení) potvrdila i práce belgických autorů [12].
Účinnost ADA na slizniční hojení hodnotila studie EXTEND. 135 pacientů bylo po indukční léčbě ADA v dávce 160/80 mg dále léčeno udržovací léčbou ADA nebo placebem. V 54. týdnu bylo kompletního slizničního hojení dosaženo u 24 % pacientů léčených ADA oproti 0 % léčených placebem [11].
Práce hodnotící účinnost anti-TNFα terapie na slizniční hojení prokazují většinou efekt léčby v oblasti tračníku a terminálního ilea, které jsou dobře přístupné koloskopickému vyšetření. Slizniční hojení CN tenkého střeva nebylo dosud důkladně studováno především z důvodu omezených diagnostických možností. Kapslová endoskopie přinesla zásadní pokrok v detekci diskrétních slizničních lézí (eroze, aftózní vředy). Senzitivita a specificita CE převyšuje všechny současné formy radiodiagnostiky v oblasti tenkého střeva [13,14]. V práci německých autorů byl počet detekovaných změn CN tenkého střeva při vyšetření CE dvojnásobný ve srovnání s počtem nálezů detekovaných CT enteroklýzou (25 vs 12/41; p < 0,005) [15]. Balonová enteroskopie má sice zásadní výhodu v možnosti odběru bioptických vzorků, je však vyšetřením méně komfortním a více rizikovým a jen výjimečně umožní vyšetření celého tenkého střeva. Obavy z použití CE u pacientů s CN budí riziko retence kapsle, která je u pacientů s potvrzenou diagnózou popisována přibližně ve 13 % vyšetření CE [16]. V našem souboru jsme tuto komplikaci zaznamenali pouze v jednom případě (2,3 %), jednalo se však o retenci dočasnou, bez nutnosti chirurgické nebo endoskopické intervence k vyjmutí kapsle. Jako prevence této komplikace se doporučuje iniciálně provést vyšetření MRI nebo CT enterografií k vyloučení těsné stenózy lumen. Alternativou těchto vyšetření by se mělo stát vyšetření retenční kapslí, výsledky jejího použití však nejsou jednoznačné [7].
K hodnocení tíže slizničních změn a určení rozsahu postižení při vyšetření CE bylo postupně vytvořeno několik indexů aktivity. Kromě indexu vytvořeného Gralnekem [8,17], který jsme použili pro potřeby naší studie, vytvořil obdobný index Gal [18]. Capsule Endoscopy Crohn’s Disease Activity Index (CECDAI) hodnotí pouze tři parametry (zánět, rozsah postižení a přítomnost stenóz) ve dvou stejných segmentech tenkého střeva, tj. v proximálním a distálním. Kvantifikace zánětlivých změn je výhodná zejména v porovnávání odpovědi na léčbu. V běžné praxi však nejsou indexy používány a zároveň nejsou k dispozici práce, které by oba indexy porovnávaly.
Mezi limity studie patří relativně malý počet nemocných a délka monitorování efektivity biologické léčby na dosažení slizničního hojení (medián 32 týdnů). Rovněž chybí srovnání s hodnotami biologických markerů (CRP, fekální kalprotektin), které by umožnilo posoudit vztah mezi hodnotou LS a laboratorními parametry zánětlivé aktivity.
Závěr
Naše práce prokázala vysokou účinnost biologické léčby protilátkami anti-TNFα v navození slizničního hojení CN tenkého střeva. Ve sledovaném souboru nemocných s relativně krátkým trváním CN tenkého střeva (medián 21 měsíců) je efekt současných biologik srovnatelný s jejich účinností ve střevě tlustém. Kapslovou endoskopii považují autoři za metodu, která je efektivní v identifikaci slizničního hojení po medikamentózní léčbě, je pacienty velmi dobře tolerována a je bezpečná. Její nevýhodou je vysoká cena a omezená úhrada ze strany zdravotních pojišťoven. Výsledky našeho sledování jsou limitovány malým počtem pacientů, k jejich potvrzení je třeba dalších studií.
Pilotní projekt byl podpořen grantem firmy Dalhausen a nadačním fondem IBD-Comfort.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 7. 2. 2013
Přijato: 9. 2. 2013
MUDr. Naděžda Machková
Klinické a výkumné centrum, ISCARE Lighthouse
Jankovcova 1569/2c
170 04 Praha 7
Zdroje
1. Bourreile A, Ignjatovic A, Aabakken E et al. Role of small bowel endoscopy in the management of patients with inflammatory bowel disease: an international OMED-ECCO consensus. Endoscopy 2009; 41 : 618–637.
2. Douda T. Kapslová endoskopie u IBD. Endoskopie 2010; 19(3–4): 117–120.
3. Tachecí I, Bureš J, Dědek P et al. Kapslová endoskopie. Nucleus HK 2008 : 180–196.
4. Kornbluth A, Colombel JF, Leigton JA et al. ICCE consensus for inflammatory bowel disease. Endoscopy 2005; 37 : 1051–1054.
5. Lewis BS. Expanding role of capsule endoscopy in inflammatory bowel disease. World J Gastroenterol 2008; 14(26): 4137–4141.
6. Efthymiou A, Viazis A, Mantzaris G et al. Does clinical response correlate with mucosal healing in patients with Crohn’s disease of small bowel? A prospective case-series study using wireless capsule endoscopy. Inflamm Bowel Dis 2008; 14(11): 1542–1547.
7. Tachecí I, Suchánek Š, Drastich P et al. Standard ČGS pro kapslovou endoskopii tenkého střeva. Gastroent Hepatol 2011; 65(4): 195–201.
8. Gralnek IM, Defrankis R, Seidman E et al. Development of a capsule endoscopy scoring index for small bowel mucosal inflammatory change. Aliment Pharmacol Ther 2008; 27(2): 146–154.
9. Froslie KF, Jahnsen J, Moum BA et al. Mucosal healing in inflammatory bowel disease: results from a Norwegian population--based cohort. Gastroenterology 2007; 133(2): 412–422.
10. Baert F, Moortgat L, Van Assche G et al. Mucosal healing predicts sustained clinical remission in patients with early stage Crohn’s disease. Gastroenterology 2010; 138(2): 463–468.
11. Van Assche G, Vermeire S, Rutgeerts P. Mucosal healing and anti TNFs in IBD. Curr Drug Targets 2010; 11(2): 227–233.
12. Schnitzler F, Fidder H, Ferrante M et al. Mucosal healing predicts long-term outcome of maitenance therapy with infliximab in Crohn’s disease. Inflamm Bowel Dis 2009; 15(9): 1295–1301.
13. Hrdlička L. Doporučený postup pro vyšetřování tenkého střeva u pacientů s Crohnovou chorobou. Gastroent Hepatol 2011; 65(2): 65–69.
14. Swain P. Wireless capsule endoscopy and Crohn’s disease. Gut 2005; 54(3): 323–326.
15. Voderholzer WA, Ortner M, Rogalla P et al. Small bowel involvement in Crohn’s disease a prospective comparison of wireless capsule endoscopy and computed tomography enteroclysis. Gut 2005; 54(3): 323–326.
16. Cheifetz AS, Kornbluth AA, Legnani P et al. The risk of retention of the capsule endoscope in patients with known or suspected Crohn’s disease. Am J Gastroenterol 2006; 101(10): 2218–2222.
17. Rosa B, Moreira MJ, Rebelo A et al. Lewis score: A useful clinical tool for patient with suspected Crohn’s disease submitted to capsule endoscopy. J Crohn Colitis 2012; 6(6): 692–697.
18. Gal E, Geller A, Fraser G et al. Assessment and validation of the new capsule endoscopy Crohn’s disease activity index (CECDAI). Dig Dis Sci 2008; 53(7): 1933–1937.
Štítky
Detská gastroenterológia Gastroenterológia a hepatológia Chirurgia všeobecná
Článok vyšiel v časopiseGastroenterologie a hepatologie
Najčítanejšie tento týždeň
2013 Číslo 1- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Fixní kombinace paracetamol/kodein nabízí synergické analgetické účinky
-
Všetky články tohto čísla
- Sérové protilátky proti zymogenovému glykoproteinu 2 (anti-GP2) u nemocných s idiopatickými střevními záněty
- Recidivující subileózní stavy na tenkém střevě mohou skýtat překvapení
- Hodnocení slizničního hojení v průběhu biologické léčby Crohnovy choroby tenkého střeva pomocí kapslové endoskopie: prospektivní observační studie
- Mesalazin u Crohnovy nemoci: obsolentní nebo neprávem opomíjená léčba?
- Současný pohled na léčbu perianálních píštělí u nemocných s Crohnovou chorobou
- Akutní krvácení do GIT a změny v lipidovém spektru – pilotní projekt
- Perforující gangrenózní cholecystitida
- Dysfunkce horní části trávicího traktu u kriticky nemocných: současný pohled a perspektiva
- 18FDG-PET/CT diagnostika adenokarcinomu pankreatu
- Stenty v liečbe zhubných nádorov kolorekta – prehľad a vlastné skúsenosti
- Metastáza maligního melanomu v bulbu duodena jako vzácná příčina obstrukce výtokového traktu žaludku
- Segmentálna portálna hypertenzia
- Plány a představy redakční rady na rok 2013
-
Imunosupresivní a biologická léčba u CN „šitá na míru“.
Komentář ke studii STORI - Aminosalicyláty v liečbe aktívnej Crohnovej choroby – kedy a prečo nie
- Komentář: Perforující gangrenózní cholecystitida
- UEGW Amsterdam 2012 – pohled z jiné strany
- Gastrofórum – Pankreatofórum v januári 2013
- Správná odpověď na kvíz
- Leading change in IBD
- Pangrol 20000
- Za vším hledej peníze (... a nebo ženu)
- Autodidaktický test: idiopatické střevní záněty
- Gastroenterologie a hepatologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Segmentálna portálna hypertenzia
- Současný pohled na léčbu perianálních píštělí u nemocných s Crohnovou chorobou
- Perforující gangrenózní cholecystitida
- Recidivující subileózní stavy na tenkém střevě mohou skýtat překvapení
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



